
2021年2月美国纽约洛克菲勒大学分子代谢实验室 Paul Cohen与Cell Metabolism发表文章Creatine-mediated crosstalk between adipocytes and cancer cells regulates obesity-driven breast cancer其研究结果证明肥胖是乳腺癌不良结果的主要危险因素。揭示了Gatm和Acsbg1是肥胖驱动的乳腺癌进展的分子调节因子。并且研究人员证明在肥胖中,肌酸是脂肪细胞和乳腺肿瘤之间相互作用的关键代谢物。
肥胖是几种癌症的风险因素,并且正迅速取代烟草成为可预防的癌症的主要原因,超重涉及15%-20%的总癌症相关死亡率。超重和肥胖的患病率在过去几十年里急剧上升,影响了美国超过70%的成年人和全球近20亿人。因此,迫切需要确定肥胖导致癌症的分子机制。在女性肥胖相关的癌症中,乳腺癌是死亡的主要原因。肥胖女性的身体质量指数(BMI)大于40,不管更年期或激素受体状态,疾病复发风险增加,相对于正常体重的女性死亡的风险增加2.12倍。三阴性乳腺癌(TNBC)是一种特别具有侵袭性的亚型,预后较差,治疗选择较少,绝经前肥胖妇女发展为三阴性乳腺癌的风险增加。
肥胖和不良乳腺癌预后之间的紧密联系的分子机制还没有被很好地理解。除了激素信号的全局性改变外,肥胖还会导致以脂肪为主的乳腺TME的局部改变,这可能会导致癌症进展。
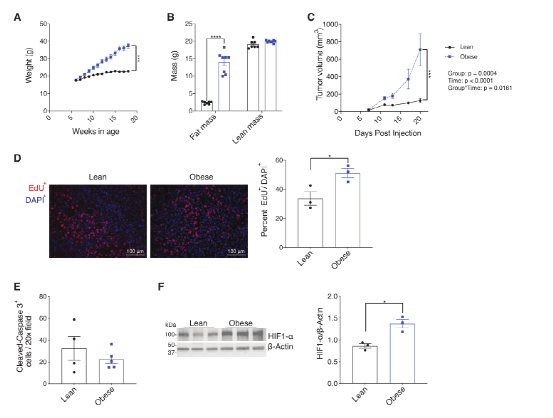
图1:在一个原位乳腺癌模型中,饮食诱导的肥胖促进肿瘤进展
研究人员试图调查乳腺脂肪细胞和乳腺癌细胞的细胞和代谢表型的协调变化是否对肥胖中肿瘤的加速进展负有责任。利用一个肥胖加速TNBC的小鼠模型,研究人员对肿瘤细胞和邻近乳腺脂肪组织进行转录组分析,以确定肥胖和乳腺癌进展之间的联系。研究人员发现了脂肪细胞特异性肌酸生物合成在促进肥胖加速肿瘤进展中的作用。这条通路通过调节癌细胞中乙酰辅酶A合成酶Acsbg1进行互补,这是一种依赖于肥胖的现象,需要完整的肌酸运输。基因表达分析两大人类军团透露,高表达的SLC6A8和Acsbg1slc6a8的高表达与无病生存期的减少有显著相关性,表明这些通路的作用在人类疾病的发病机制。这里提供的数据定义了一个以肌酐代谢为中心的迄今为止难以描述的途径,该途径驱动脂肪细胞和癌细胞之间的交流,在肥胖的特定背景下。
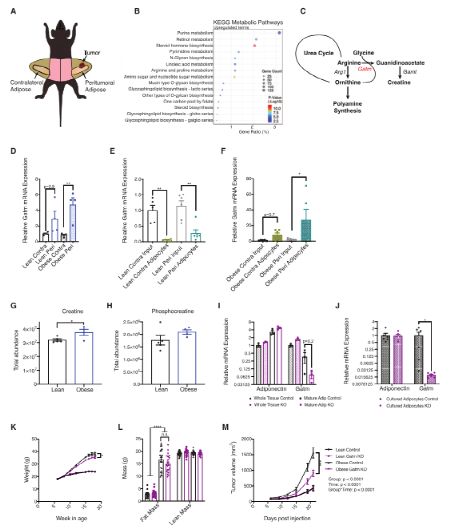
图2:肥胖加速乳腺癌模型脂肪组织的转录组分析
在美国,每8名女性中就有1人患乳腺癌,每年导致4万多人死亡(CDC, 2019)。肥胖是乳腺癌发病率和疾病预后恶化的主要危险因素,但这些观察结果背后的机制尚未完全阐明。研究人员假设在TME中脂肪组织和癌细胞之间的相互作用可能导致肥胖驱动的乳腺癌进展。使用肥胖促进型乳腺癌的小鼠模型,研究人员对瘤周脂肪组织和肿瘤细胞进行了综合分析,发现了一个以前未描述的途径,其中脂肪细胞的肌酸代谢影响肿瘤或进展,令人惊讶的是,这些影响似乎是肥胖特异性的,与癌细胞将脂肪酸转化为酰基辅酶a的能力有关。
由于在体外无法完全概括的大量系统和组织水平变化的肥胖结果,研究人员利用多种活体模型来分析这一途径与乳腺癌进展的相关性。研究人员通过脂肪细胞特异性基因缺失gatm证明,脂肪细胞来源的肌酸对肥胖驱动的乳腺癌进展至关重要。有趣的是,在瘦或肥胖动物中,膳食中添加肌酸并不能促进肿瘤的生长,这表明TME中的肌酸,而不是全身肌酸,在该模型中起着促进乳腺癌进展的重要作用。此外,不表达肌酸转运体的癌细胞在体内完全消融了肥胖加速的肿瘤生长,这表明在肥胖中需要外源肌酸促进肿瘤生长。研究人员的实验表明,在肥胖动物中乳腺癌细胞过表达Acsbg1,高Acsbg1表达促进肥胖驱动的肿瘤在肌酸依赖的mannerin体内进展,提示了这种肌酸穿梭的意义。这种依赖性与癌细胞中高能磷酸盐池的扩张有关,这可能最终通过提供细胞增殖所需的能量来驱动肿瘤的进展。总之,这些发现揭示了中枢肌酸代谢减少促进肥胖加速乳腺癌进展的作用。
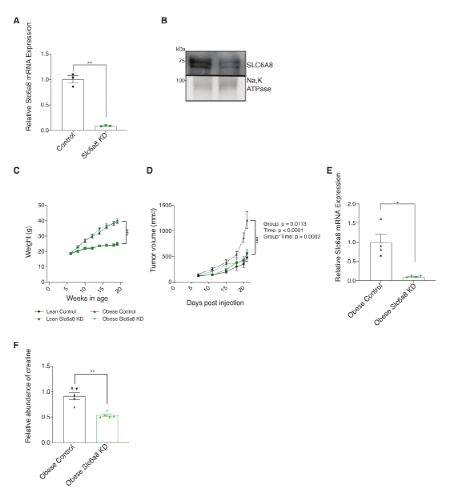
图3:乳腺癌细胞中肌酸转运蛋白(Slc6a8)的基因敲低降低了肥胖患者的肿瘤生长
研究人员提出了一种机制,在肿瘤存在时,肥胖脂肪细胞通过代谢重编程来增强肌酸的产生(图6F)。引起这种变化的信号尚不清楚,这将是未来研究的一个丰富领域。同时,肥胖微环境中的癌细胞上调了Acsbg1,它通过氧化磷酸化促进ATP的产生,并通过SLC6A8增强了来自TME的脂肪细胞源性肌酸的输入。细胞内ATP和肌酸浓度的增加支持磷酸肌酸的产生,这可能通过确保在肿瘤缺氧期间继续合成代谢过程而促进肿瘤进展。研究人员已经用氘化肌酸实验证明,培养的乳腺癌细胞可以吸收肌酸生成磷酸肌酸。虽然SLC6A8被提出同时转运肌酸和磷酸肌酸,但这从未被直接证明,而且脂肪细胞和癌细胞都具有将肌酸转化为磷酸肌酸的机制。肌酸激酶/磷酸肌酸电路有很好的描述角色在维持高水平的ATP期间增加的能源需求,如肌肉收缩或快速增殖,并以前涉及肿瘤恶化的模型,包括her2阳性乳腺癌。对另一种与肥胖相关的癌症——结直肠癌的进一步研究揭示了通过SLC6A8导入外源性磷酸肌酸,以满足肝脏转移定植的高能量需求的重要作用。这些发现与人类疾病的相关性由来自两个人类乳腺癌队列的基因表达分析证实。
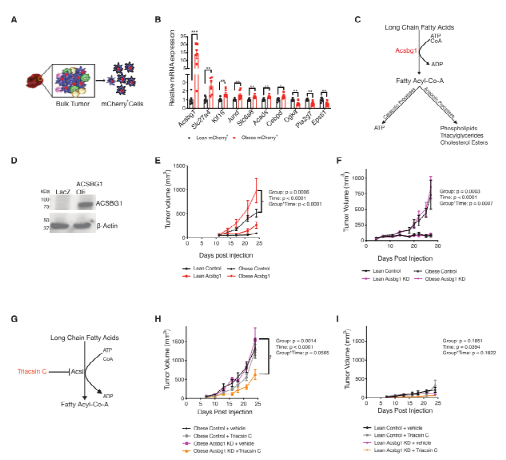
图4:瘦和肥胖肿瘤细胞的转录组分析
在超重和过度肥胖的患者中,高表达的slc6a8和Acsbg1与更具侵略性的三阴性基础亚型相关。此外,SLC6A8和Acsbg1的高表达与较差的肿瘤分级相关,无论其亚型如何,而SLC6A8的表达与TNBC患者的预后较差相关。这些数据支持对靶向slc6a8和Acsbg1的预后和治疗潜力的进一步研究,特别是在肥胖患者中。尽管肥胖和非肥胖患者的治疗结果有公认的差异,但目前的护理标准对两组患者提供了相同的治疗。不仅针对肿瘤特异性分子靶点,而且针对患者特征(如肥胖)的定制治疗的能力将代表个性化药物的重大进步。
在过去的几个阶段中,乳腺癌的检测和治疗的进步导致了预后的显著改善;然而,乳腺癌仍然是世界范围内发病率和死亡率的主要原因。此外,肥胖率的迅速上升,这是乳腺癌预后恶化的既定危险因素,可能会破坏为减轻这种疾病的负担所取得的进展。研究人员的工作表明,靶向肌酸代谢可能是一种有吸引力的治疗策略,可以减轻肥胖对这一乳腺癌脆弱人群肿瘤进展的不利影响。此外,这里提供的数据发现肌酸在促进肥胖依赖性肿瘤生长中的重要作用,并为进一步研究肌酸代谢在其他肥胖驱动的癌症类型中的作用提供了基础。
原文链接:
https://doi.org/10.1016/j.cmet.2021.01.018













